💎 فهرست مطالب
وقتی یک مولکول هم با آب دوست است و هم با روغن، چه اتفاقی میافتد؟
این همان لحظهای است که علم شیمی با جادوی عملکرد مولکول های آمفی فیلیک به اوج میرسد. از قدرت تمیزکنندگی صابونها و شامپوها گرفته تا ساختارهای بنیادین حیات در غشاهای سلولی و رسانش دارو در نانوپزشکی، همه اینها بر پایه یک ویژگی ساده اما خارقالعاده بنا شدهاند: دوگانگی قطبیت در یک مولکول.
در این مقاله، با دنیای شگفتانگیز آمفی فیلیکها آشنا میشویم؛ مولکول هایی با دو چهره—آب دوست و چربی دوست—که می توانند مرز بین دنیای آبی و چربی را درنوردند. از نحوه تشکیل میسلها و امولسیون ها تا نقش حیاتی آنها در زیست شناسی و صنایع آرایشی، با ما همراه باشید تا دریابید چگونه این مولکول های کوچک، نقشی بزرگ در زندگی روزمره و فناوری های پیشرفته ایفا میکنند.
خصلت آمفی فیلیک چیست؟
آمفی فیلیک، از واژه یونانی “amphis” به معنای “هر دو” و “philia” به معنای “دوستی” یا “عشق” برگرفته شده است. یک ترکیب شیمیایی آمفی فیلیک، یا به عبارت دیگر آمفی پاتیک، ترکیبی است که دارای هر دو ویژگی آبدوست (هیدروفیلیک) و چربیدوست (لیپوفیلیک) یا آبگریز (هیدروفوبیک) است. این دوگانگی در یک مولکول واحد، آن را قادر میسازد تا همزمان با محیطهای آبی و غیرآبی تعامل کند.
بخش های آب دوست و آب گریز/چربیدوست
مولکولهای آمفی فیلیک دارای دو بخش مشخص هستند:
- بخش آبدوست (هیدروفیلیک): این قسمت از مولکول به آب جذب میشود زیرا قطبی است. گروههای قطبی میتوانند شامل گروههای باردار باشند. مثالهایی از گروههای آنیونی، که بخش لیپوفیلیک مولکول با R نشان داده میشود، عبارتند از:
- کربوکسیلاتها: RCO2−
- سولفاتها: RSO4−
- سولفوناتها: RSO3−
- فسفاتها (گروه عملکردی باردار در فسفولیپیدها) همچنین گروههای کاتیونی نیز وجود دارند، مانند:
- آمونیومها: RNH3+ علاوه بر این، گروههای قطبی بدون بار نیز شامل میشوند. مثالها عبارتند از الکلها با گروههای R بزرگ، مانند دیاسیل گلیسرول (DAG) و الیگو اتیلن گلیکول با زنجیرههای آلکیل بلند. این بخش “سر” مولکول آمفی فیلیک را تشکیل میدهد.
- بخش چربیدوست/آبگریز (لیپوفیلیک/هیدروفوبیک): این قسمت از مولکول آب را دفع کرده و به چربیها و روغنها تمایل دارد زیرا غیرقطبی است. این بخش معمولاً یک زنجیره هیدروکربنی بزرگ است، مانند CH3(CH2)n که در آن n > 4. این قسمت “دم” مولکول آمفی فیلیک را تشکیل میدهد.
اغلب، گونههای آمفی فیلیک چندین بخش چربیدوست، چندین بخش آبدوست یا هر دو را دارند. پروتئینها و برخی کوپلیمرهای بلوکی نمونههایی از این موارد هستند. در نتیجهی داشتن هر دو بخش چربیدوست و آبدوست، برخی از ترکیبات آمفی فیلیک ممکن است در آب و تا حدی در حلالهای آلی غیرقطبی حل شوند. هنگامی که در یک سیستم دوفازی نامحلول شامل حلالهای آبی و آلی قرار میگیرند، ترکیب آمفی فیلیک بین دو فاز توزیع میشود. میزان توزیع توسط وسعت بخشهای هیدروفوبیک و هیدروفیلیک تعیین میشود.
مکانیزم عملکرد: چگونه آمفی فیلیکها کار میکنند؟
نحوهی عملکرد مولکولهای آمفی فیلیک در محیطهای مختلف، به خصوص در حضور آب و روغن/چربی، آنها را به عوامل پاککننده و امولسیون کننده قدرتمندی تبدیل میکند.
تشکیل میسل توسط مولکولهای آمفی فیلیک
یکی از مهمترین ویژگیهای مولکولهای آمفی فیلیک، توانایی آنها در تشکیل ساختارهایی به نام میسل (micelle) در محلولهای آبی است. میسلها ساختارهای کروی هستند که در یک محلول آبی هنگامی که غلظت مولکولهای آمفی فیلیک، مانند صابون، به نقطهی خاصی معروف به غلظت بحرانی میسل (Critical Micelle Concentration یا CMC) میرسد، تشکیل میشوند. ساختار میسل به این صورت است که دمهای آبگریز مولکولها (بخشهای هیدروفوبیک) به سمت داخل تجمع کرده و از آب پنهان میشوند، در حالی که سرهای آبدوست آنها (بخشهای هیدروفیلیک) به سمت بیرون قرار گرفته و با محیط آبی در تماس هستند. این آرایش باعث به حداقل رسیدن انرژی سیستم میشود، زیرا دمهای آبگریز از مولکولهای آب دور نگه داشته میشوند. میسلها معمولاً کروی شکل هستند، اما بسته به تعداد و ترکیب مولکولها، ممکن است اشکال بیضی یا استوانهای نیز به خود بگیرند. بر خلاف تصویرسازی متداول، میسلها معمولاً توسط آمفی فیلیکهای غیربیولوژیکی و تکزنجیرهای مانند صابونها یا شویندهها تشکیل میشوند، زیرا جای دادن دو زنجیره در این شکل دشوار است.
امولسیون سازی توسط مولکولهای آمفی فیلیک
امولسیون سازی فرآیندی است که در آن دو مایع غیرقابل اختلاط، مانند آب و روغن، وادار به مخلوط شدن و تشکیل یک مخلوط پایدار میشوند. صابون به عنوان یک عامل امولسیونکننده عمل میکند و مخلوط را با کاهش کشش سطحی در مرز مشترک روغن و آب پایدار میکند. هنگامی که صابون یا شوینده در آب حل میشود و با روغن یا چربی تماس پیدا میکند، دمهای آبگریز مولکولهای آمفی فیلیک، روغن یا چربی را احاطه میکنند. در همین حال، سرهای آبدوست به سمت آب قرار میگیرند. این عمل باعث میشود که روغن به قطرات بسیار کوچکتری تجزیه شده و این قطرات توسط میسلها در داخل خود محبوس شوند. این ساختار (میسل حاوی روغن/کثیفی) اکنون در آب محلول شده و میتواند به راحتی با آب شسته شود. این مکانیسم بنیادی، اساس قدرت پاککنندگی صابونها و شویندهها است. به عبارت دیگر، صابون به دلیل اینکه هم به روغن و هم به آب قویتر از خودش پیوند میخورد، تمایل به حل شدن پیدا میکند و روغن و کثیفی را با خود میشوید. فوم یا کفی که هنگام شستشوی دستها ظاهر میشود، حاوی این ساختارهای روغنی است که در نهایت از دست شما شسته میشوند. از آنجایی که سرهای آبدوست میسل در آب محلول هستند، میتوانند شسته شوند؛ بنابراین هنگامی که صابون را با آب میشویید، صابون روغن حاوی میکروب را با خود حمل میکند و این به معنای رفتن آن به داخل سینک است.
توزیع مولکولهای آمفی فیلیک در سیستمهای دوفازی
همانطور که ذکر شد، مولکولهای آمفی فیلیک قادرند در سیستمهای دوفازی (آبی و آلی) بین دو فاز توزیع شوند. میزان توزیع بستگی به نسبت بخشهای آبگریز و آبدوست مولکول دارد. این خاصیت برای بسیاری از کاربردها، از جمله در فرمولاسیون محصولات که نیاز به مخلوط کردن فازهای روغنی و آبی دارند، بسیار مهم است.
مولکولهای آمفی فیلیک در بیولوژی
خصلت آمفی فیلیک نه تنها در شیمی و صنعت، بلکه در سیستمهای بیولوژیکی نیز نقشهای حیاتی ایفا میکند. این ویژگی اساس ساختار و عملکرد بسیاری از اجزای سلولی و فرایندهای زیستی است.
غشاهای بیولوژیکی: بنیان حیات
یکی از مهمترین کاربردهای خصلت آمفی فیلیک در طبیعت، ساختار غشاهای بیولوژیکی، از جمله غشای سلولی است. غشای سلولی یا غشای پلاسمایی، لایهی خارجی سلولها است که سلول را از محیط اطرافش جدا میکند. فسفولیپیدها، که بخش عمدهای از غشاهای سلولی را تشکیل میدهند، مولکولهایی آمفی فیلیک هستند و اصلیترین اجزای تشکیلدهندهی غشاهای بیولوژیکی محسوب میشوند. هر فسفولیپید از یک سر قطبی (یک گروه فسفات با بار منفی) و دو دم غیرقطبی (دو زنجیره اسید چرب) تشکیل شده است. این ساختار منحصر به فرد باعث میشود که فسفولیپیدها در محیطهای آبی به طور طبیعی یک ساختار دولایه تشکیل دهند که به آن دولایه لیپیدی (lipid bilayer) میگویند. در این ساختار، سرهای آبدوست به سمت محیط آبی بیرون و داخل سلول قرار میگیرند، در حالی که دمهای آبگریز به سمت یکدیگر در مرکز دولایه قرار میگیرند و یک ناحیه غیرقطبی را تشکیل میدهند. این ساختار انعطافپذیر و نیمهنفوذپذیر، سلول را از محیط اطرافش جدا کرده و جریان مواد غذایی و سیگنالهای بیوشیمیایی را به طور انتخابی کنترل میکند. ضخامت غشای سلولی به طور کلی حدود ۷ تا ۱۰ نانومتر است و پروتئینها حدود ۵۰ درصد از وزن بیشتر غشاهای سلولی را تشکیل میدهند. علاوه بر فسفولیپیدها، سایر مولکولهای آمفی فیلیک مانند کلسترول و گلیکولیپیدها نیز در ساختار غشاهای بیولوژیکی حضور دارند و خواص فیزیکی و بیولوژیکی متفاوتی به آنها میبخشند. به عنوان مثال، کلسترول که خود یک مولکول آمفی پاتیک است، با زنجیرههای اسید چرب فسفولیپیدها برهمکنش میدهد و سیالیت غشا را تنظیم میکند و از کریستالیزه شدن آن جلوگیری مینماید. بخش قطبی کلسترول را گروه OH میسازد و بقیه مولکول کلسترول بخش غیرقطبی آن را تشکیل میدهند.
نقش آمفی فیلیک در فرایندهای بیولوژیکی
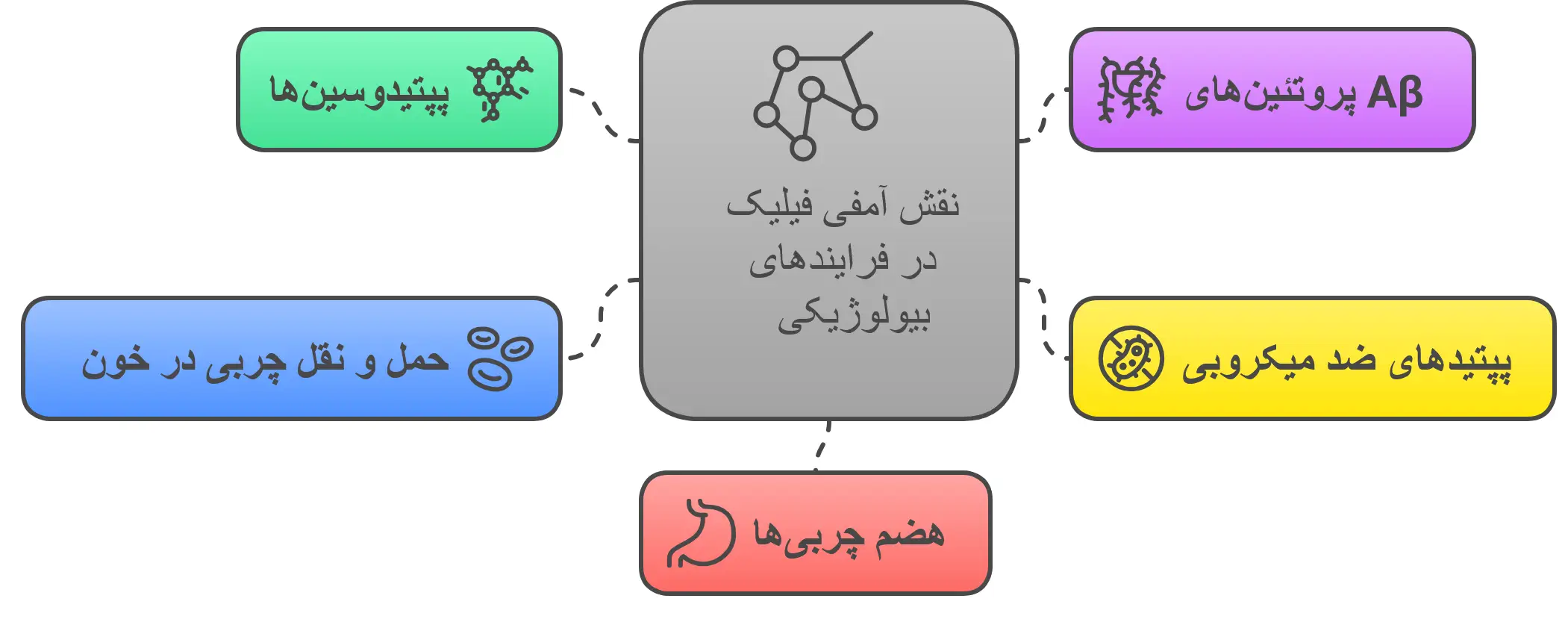
مولکولهای آمفی فیلیک فراتر از ساختار غشایی، در بسیاری از فرایندهای بیولوژیکی دیگر نیز شرکت دارند:
- پپتیدوسینها (Pepducins): این ترکیبات آمفی فیلیک به شدت با غشاهای بیولوژیکی تعامل میکنند. بخش آبگریز آنها به درون غشای لیپیدی وارد شده و بخش آبدوست آنها به سمت محیط آبی قرار میگیرد. این عمل میتواند رفتار فیزیکی غشا را تغییر داده و گاهی اوقات آن را مختل کند.
- پروتئینهای Aβ (آمیلوئید بتا): پروتئینهای Aβ ورقههای بتا ضد موازی قوی آمفی فیلیک را تشکیل میدهند که تجمع یافته و فیبریلهای سمی اکسیداتیو Aβ را ایجاد میکنند. فیبریلهای Aβ خود از ساندویچهای بتای مدولار ۱۳-مری آمفی فیلیک که با چرخشهای معکوس از هم جدا شدهاند، تشکیل شدهاند.
- پپتیدهای ضد میکروبی (Antimicrobial Peptides – AMPs): این پپتیدها دستهای دیگر از مولکولهای آمفی فیلیک هستند. یک تحلیل داده بزرگ نشان داد که آمفی پاتیسیته بهترین عامل تمایز بین AMPهایی با فعالیت ضد باکتری گرم منفی و بدون آن است. هر چه آمفی پاتیسیته بیشتر باشد، شانس AMPها برای داشتن فعالیت دوگانه ضد باکتری و ضد قارچی بهتر است.
- حمل و نقل چربی در خون: برخی پروتئینها در خون، مانند آلبومین، نیز خواص آمفی فیلیک دارند و به اتصال و انحلال چربیها کمک میکنند تا امکان انتقال آنها در سراسر جریان خون فراهم شود.
- هضم چربیها: اسیدهای صفراوی، که از استروئیدهای آمفی پاتیک هستند، برای هضم چربیهای غذایی ضروری هستند. آنها به تشکیل میسلها در روده کمک میکنند تا چربیها جذب سلولهای رودهای شوند.
آمفی فیلیکها در صنعت: از پاککنندگی تا پزشکی
کاربرد خصلت آمفی فیلیک به هیچ وجه به حوزهی بیولوژی محدود نمیشود و در صنایع مختلف، به خصوص در تولید محصولات شیمیایی مصرفی، نقش کلیدی دارد.
صابونها و شویندهها
صابون یک ترکیب آمفی فیلیک سورفکتانت رایج خانگی است. هنگامی که صابون با آب (قطبی، آبدوست) مخلوط میشود، برای پاک کردن روغنها و چربیها (غیرقطبی، چربیدوست) از ظروف آشپزخانه، لباس و پوست بسیار مفید است. این کار از طریق تشکیل میسلها و امولسیونسازی صورت میگیرد که پیشتر توضیح داده شد. اثربخشی صابون به عنوان یک عامل پاککننده، به دلیل ساختار مولکولی آمفی فیلیک منحصربهفرد آن است، که شامل یک زنجیرهی هیدروکربنی آبگریز و یک سر قطبی آبدوست میباشد. این ساختار به صابون اجازه میدهد تا هم در آب و هم در چربیها حل شود، میسل تشکیل دهد و چربی و کثیفی را امولسیون کند. میسلهای صابون ذرات کثیفی یا قطرات چربی را احاطه کرده و آنها را امولسیون میکنند و در آب محلول میسازند. هنگامی که محلول صابون آبکشی میشود، میسلهای حاوی کثیفی نیز شسته شده و سطحی تمیز باقی میماند.
محصولات آرایشی و بهداشتی
سورفکتانتها (مولکولهای آمفی فیلیک) در صنعت آرایشی و بهداشتی کاربردهای بی شماری دارند و در محصولاتی مانند شامپوها، ژلهای دوش، پاککنندههای صورت، نرمکنندهها و ماسکهای مو ضروری هستند. وظایف اصلی آنها عبارتند از:
- امولسیون کنندهها: کمک به حفظ اختلاط فازهای روغن و آب در کرمها، لوسیونها و نرمکنندهها.
- شویندهها: حذف مؤثر روغنها و ناخالصیها از پوست یا مو.
- حلالکنندهها (Solubilizers): امکان ترکیب مقادیر کمی از روغنهای اساسی یا سایر مواد چربیدوست را در پایههای آبی فراهم میکنند.
- نرمکنندهها: افزایش نرمی و قابلیت مدیریت مو.
سورفکتانتهای آرایشی بر اساس بار الکتریکی سر آبدوستشان در آب به چهار نوع اصلی تقسیم میشوند:
- سورفکتانتهای آنیونی: این سورفکتانتها دارای بار منفی هستند و بیشترین استفاده را در محصولات پاککننده مانند شامپوها و ژلهای دوش دارند. توانایی قوی آنها در پاککنندگی، روغنها و کثیفیها را به طور مؤثری از بین میبرد و کف زیادی تولید میکنند. با این حال، قدرت آنها گاهی میتواند منجر به تحریک پوست یا سر شود، بنابراین اغلب با سورفکتانتهای ملایمتر ترکیب میشوند تا اثرات آنها متعادل شود.
- نمونهها: سدیم لوریل سارکوزینات، سدیم کوکویل گلوتامات، سدیم لوریل گلوتامات، سدیم متیل کوکویل تائورات، سدیم کوکویل ایزتیونات، سدیم کوکویل گلیسینات.
- سورفکتانتهای آمفوتری: این سورفکتانتها توانایی منحصر به فردی در تغییر بار خود بسته به pH محیط دارند، که آنها را بسیار متنوع میسازد. آنها ملایمتر از سورفکتانتهای آنیونی هستند و پاککنندگی ملایمی با خواص کفکنندگی خوب ارائه میدهند، که آنها را برای پوستهای حساس یا محصولات کودک ایدهآل میکند.
- نمونهها: کوکو بتائین، کوکامیدوپروپیل بتائین، دیسدیم کوکوآمفودیاستات.
- سورفکتانتهای غیریونی: این سورفکتانتها فاقد بار الکتریکی هستند و در نتیجه، عملکرد بسیار ملایمی روی پوست دارند. اگرچه توانایی پاککنندگی و کفکنندگی کمتری دارند، اما تحریکپذیری پایین آنها باعث میشود برای محصولات آرایشی طبیعی یا ارگانیک مناسب باشند. آنها همچنین به طور رایج به عنوان امولسیونکننده برای پایداری کرمها و لوسیونها استفاده میشوند.
- نمونهها: کاپریلویل/کاپرویل متیل گلوکامید، کوکویل متیل گلوکامید، لوریل/میزیریل متیل گلوکامید، لوریل/میزیریل متیل گلوکامید و کوکو-بتائین، کاپریلویل/کاپرویل متیل گلوکامید و لوریل/میزیریل متیل گلوکامید، سانفلاوروئیل متیلگلوکامید.
- سورفکتانتهای کاتیونی: این سورفکتانتها دارای بار مثبت هستند و عمدتاً در محصولات مراقبت از مو مانند نرمکنندهها و ماسکها استفاده میشوند. وظیفه اصلی آنها پاککنندگی نیست، بلکه نرمکنندگی است، زیرا به کاهش الکتریسیته ساکن، بهبود شانه پذیری و نرمتر شدن مو کمک میکنند. آنها کف تولید نمیکنند و در فرمولاسیونهای پاککننده استفاده نمیشوند، اما در محصولاتی که هدف آنها ترمیم یا محافظت از مو است، ضروری هستند.
- نمونهها: بهنتریمونیوم کلرید، بهنتریمونیوم متوسولفات.
روند کنونی در صنعت آرایشی و بهداشتی به سمت افزایش تقاضای مصرفکنندگان برای لوازم آرایشی طبیعی و پایدار است، که منجر به افزایش علاقه به سورفکتانتهای زیستتخریبپذیر و گیاهی میشود. موادی مانند گلوکوزیدها (مشتقات شکر) و سورفکتانتهای بر پایه نارگیل، جایگزینهای عالی برای سولفاتهای سنتی هستند و با روند فرمولاسیونهای دوستدار محیط زیست همخوانی دارند.
نانوپزشکی: یک مرز در رسانش دارو
خصلت آمفی فیلیک حتی در حوزههای پیشرفته مانند نانوپزشکی نیز کاربرد پیدا کرده است. نانوپزشکی به کارگیری فناوری نانو برای امور پزشکی است که در تشخیص، پیشگیری و بهبود بیماران به کار میرود. یکی از چالشهای اصلی در درمان بیماریها، به ویژه سرطان، این است که بسیاری از داروهای شیمی درمانی به دلیل ماهیت آبگریز خود، فراهمی زیستی (bioavailability) محدودی دارند، یعنی به اندازه کافی به بافتهای هدف نمیرسند یا در بدن پایدار نیستند. محققین به دنبال روشهایی هستند که حلالیت و ثبات شیمیایی این ترکیبات را برای کاربردهای بالینی افزایش دهند.
نانوپزشکی با استفاده از حاملهای دارویی نانومقیاس با ویژگیهای آمفی فیلیک، این مشکل را حل میکند. این حاملها، مانند نانوذرات، میسلهای پوشیده از سیلیس و لیپوزومهای دارای پیوند عرضی (که خود ساختارهای آمفی پاتیک دولایهای هستند)، میتوانند داروهای آبگریز را در هسته آبگریز خود کپسوله کرده و در عین حال با محیط آبی بدن سازگار باشند. یکی از نمونههای مطالعاتی در این زمینه، سنتز نانوحاملهای متشکل از پلیمرهای آلژینات-کیتوسان-پلورونیک F127 است که به عنوان یک ترکیب پلیمری آمفی فیلیک سنتز شده و برای انتقال کورکومین (یک ترکیب گیاهی آبگریز) به سلولهای سرطان سرویکال انسان استفاده شده است. نتایج این مطالعه نشان داد که استفاده از نانوحاملهای آمفی فیلیک میتواند روشی کارآمد برای انتقال داروهای آبگریز باشد و کاربرد این ترکیبات را در درمان سرطان افزایش دهد. این رویکرد به ویژه در هدفگیری سلولهای سرطانی مفید است، زیرا میتواند سمیت داروها را برای سلولهای سالم کاهش دهد و فراهمی زیستی آنها را در بافتهای سرطانی افزایش دهد.
چشمانداز آینده و تحقیقات
تحقیقات در زمینه مولکولهای آمفی فیلیک همچنان در حال پیشرفت است. دانشمندان به دنبال طراحی مولکولهایی با خواص آمفی فیلیک دقیقتر برای کاربردهای خاص هستند، از جمله:
- بولاآمفی فیلیکها: ترکیباتی که دارای گروههای آبدوست در هر دو انتهای مولکول هستند. این مولکولها میتوانند میسلهای پرولیت (کشیده) تشکیل دهند و حلالیت بیشتری در آب نسبت به آمفی فیلیکهای تکسر دارند.
- مطالعات ترمودینامیکی: بررسی ویژگیهای ترمودینامیکی (مانند انرژی آزاد، آنتالپی، آنتروپی) انتقال آمفی فیلیکها بین فازهای آب و غشا، به درک عمیقتر برهمکنشها و طراحی مولکولهای کارآمدتر کمک میکند. مطالعات انجام شده بر روی لیپوپپتیدهای آمفی فیلیک نشان داده است که ورود آنها به غشا بیشتر از طریق آنتالپی هدایت میشود تا اثرات آنتروپیک حلال.
- پروتئینهای آمفی فیلیک: پروتئینها و برخی کوپلیمرهای بلوکی نیز میتوانند آمفی فیلیک باشند و در زمینههای مختلف بیوشیمیایی و پزشکی مورد مطالعه قرار میگیرند.
- پپتیدهای ضد میکروبی: تحقیقات گستردهای در مورد افزایش کارایی و کاهش سمیت این پپتیدها از طریق بهینهسازی آمفی پاتیسیته آنها در حال انجام است.
این تحقیقات نه تنها به بهبود محصولات فعلی کمک میکنند، بلکه در را به روی نوآوریهای جدید در زمینههایی مانند پزشکی دقیق، مواد هوشمند و پایداری زیستمحیطی باز میکنند.
نتیجهگیری
خصلت آمفی فیلیک یک ویژگی مولکولی قدرتمند است که اساس عملکرد طیف وسیعی از مواد و فرایندها را در طبیعت و صنعت تشکیل میدهد. از نقش حیاتی فسفولیپیدها در ساختار غشاهای سلولی گرفته تا عملکرد صابونها به عنوان عوامل پاککننده، و همچنین کاربردهای نوآورانه در نانوپزشکی برای رسانش دارو، این مفهوم پایه و اساس درک ما از تعاملات مولکولی در سیستمهای پیچیده است. اثربخشی صابون به عنوان یک عامل پاککننده، به دلیل ساختار مولکولی آمفی فیلیک منحصر به فرد آن است، که به آن اجازه میدهد تا میسل تشکیل داده و چربی و کثیفی را امولسیون کند، و آنها را به راحتی در آب محلول و قابل حذف از سطوح سازد. برای سازندگان صابون و فعالان در صنعت محصولات آرایشی و بهداشتی، تسلط بر این دانش به معنای توانایی بیشتر در فرمولهسازی محصولات مؤثرتر، ایمنتر و نوآورانهتر است. با درک دقیق نحوه عملکرد سر و دم آبدوست و آبگریز، شما میتوانید بهترین سورفکتانتها را انتخاب کنید، پایداری امولسیونها را بهبود بخشید و در نهایت، محصولاتی تولید کنید که نیازهای مصرفکنندگان را به بهترین شکل ممکن برآورده سازند.
سوالات متداول (FAQ)
آمفی فیلیک دقیقاً به چه معناست؟
آمفی فیلیک به یک ترکیب شیمیایی اطلاق میشود که همزمان دارای بخشهای آبدوست (هیدروفیلیک یا قطبی) و چربیدوست (لیپوفیلیک یا آبگریز و غیرقطبی) است. این دوگانگی به مولکول اجازه میدهد تا با هر دو محیط آبی و روغنی تعامل داشته باشد. مثال بسیار خوبی از این نمونه، مایع ظرفشویی است.
صابونها چگونه کثیفی و روغن را پاک میکنند؟
مولکولهای صابون آمفی فیلیک هستند؛ یعنی یک سر آبدوست و یک دم آبگریز دارند. دمهای آبگریز به ذرات روغن و کثیفی میچسبند، در حالی که سر آبدوست با آب در تماس است. این باعث میشود که روغن و کثیفی به صورت میسلهای کوچک در آب معلق شده و به راحتی با شستشو از سطح جدا شوند.
نقش آمفی فیلیکها در غشای سلولی چیست؟
فسفولیپیدها، که اجزای اصلی غشاهای سلولی هستند، مولکولهای آمفی فیلیک هستند. آنها به طور طبیعی در یک محیط آبی خود را به صورت یک دولایه (دولایه لیپیدی) سازماندهی میکنند. در این ساختار، سرهای آبدوست به سمت محیط آبی بیرونی و درونی سلول قرار میگیرند، و دمهای آبگریز در مرکز دولایه به هم میپیوندند و یک سد انتخابی برای سلول ایجاد میکنند.
آیا انواع مختلفی از سورفکتانتهای آمفی فیلیک وجود دارد؟
بله، سورفکتانتهای آمفی فیلیک بر اساس بار الکتریکی سر آبدوستشان در آب به چهار دسته اصلی تقسیم میشوند: آنیونی (با بار منفی)، کاتیونی (با بار مثبت)، غیریونی (بدون بار) و آمفوتری (که میتوانند بار مثبت یا منفی داشته باشند بسته به pH محیط). هر نوع کاربرد خاصی در صنایع مختلف، از جمله محصولات پاککننده و آرایشی، دارد.
چرا خصلت آمفی فیلیک برای ساخت محصولات آرایشی مهم است؟
در محصولات آرایشی و بهداشتی، مولکولهای آمفی فیلیک به عنوان امولسیونکننده عمل میکنند تا فازهای روغن و آب را مخلوط و پایدار نگه دارند (مانند کرمها و لوسیونها). آنها همچنین به عنوان شویندهها برای پاکسازی پوست و مو، حلالکنندهها برای ترکیب مواد روغنی در پایههای آبی، و نرمکنندهها برای بهبود بافت مو استفاده میشوند.
نانوپزشکی چگونه از مولکولهای آمفی فیلیک استفاده میکند؟
نانوپزشکی از مولکولهای آمفی فیلیک برای ساخت نانوحاملها (مانند لیپوزومها و نانوذرات) برای رسانش دارو استفاده میکند. این نانوحاملها میتوانند داروهای آبگریز را کپسوله کرده و آنها را به طور مؤثرتری به بافتهای هدف در بدن برسانند و فراهمی زیستی دارو را افزایش دهند، که به ویژه در درمان سرطان اهمیت دارد.
رفع مسئولیت پزشکی
توجه: مطالب این وبسایت جنبه اطلاعرسانی داشته و جایگزین معاینه و تشخیص پزشک نیست. هرگز بدون مشورت با متخصص، دارو مصرف نکنید یا درمان خود را تغییر ندهید.


نظرات (0)
هنوز نظری ثبت نشده است. اولین نفر باشید!
ثبت نظر جدید